1. Definició de matèria
Des d'un punt de vista físic, la matèria és el constituent de totes les substàncies. Tant dels planetes com dels éssers vius, de tots els objectes, de l'aire o de l'aigua; i d'altres formes com la llum i la radiació electromagnètica.
De fet, la paraula matèria esta relacionada amb el terme llatí mäter que significa "origen, font, mare".
De fet, la paraula matèria esta relacionada amb el terme llatí mäter que significa "origen, font, mare".
En el context de la física moderna, trobem la matèria màssica i la matèria no màssica. En aquest tema, fem únicament referència a la matèria màssica: tot allò que ocupa un lloc a l'espai i té massa. Per tant, és observable, mesurable i capaç d'interaccionar.
2. Composició de la matèria
Nivell macroscòpic
D'acord amb la teoria cinètica molecular, la matèria es troba formada per partícules molt petites (molècules) que s'atreuen entre elles i es mouen contínuament.
La mobilitat de les partícules depèn de la temperatura, de manera que a mes temperatura, mes moviment tenen les partículas. Aquest grau de mobilitat és el factor que determina les propietats de la matèria i també justifica els canvis d'estat.
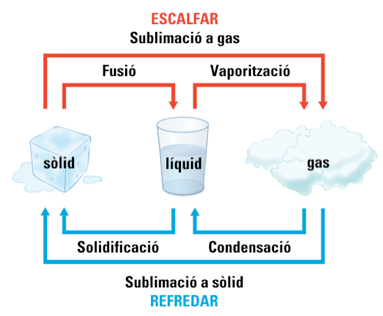
En física i química, s'anomena canvi d'estat a l'evolució de la matèria entre diversos estats d'agregació sense que hi hagi canvis en la seva composició.
Segons la teoria cineticomol.lecular explicada anteriorment, el paràmetre del qual depèn un cos per què es trobi en un estat o en un altre, és la temperatura, i també afavoreix la pressió:
Propietats generals
LA MASSA (m)
EL VOLUM (V)
LA TEMPERATURA (Tª)
Propietats específiques o característiques
EL PUNT DE FUSIÓ I D'EBULLICIÓ
EL COLOR, L'OLOR I EL SABOR
ALTRES PROPIETATS ESPECÍFIQUES:
La composició de la matèria màssica està organitzada en diversos nivells i pot ser estudiada des dels punts de vista microscòpic i macroscòpic.
Nivell microscòpic
Microscòpicament, la matèria màssica pot entendre's com un agregat de molècules. Aquestes són agrupacions d'àtoms que formen part del nivell microscòpic.
Els àtoms són partícules que trobem directament a la natura. Ara per ara, s'han descobert 118 àtoms diferents, que constitueixen els elements químics i que es disposen de manera ordenada, a la taula periòdica
Els àtoms són partícules que trobem directament a la natura. Ara per ara, s'han descobert 118 àtoms diferents, que constitueixen els elements químics i que es disposen de manera ordenada, a la taula periòdica
 |
| La taula periòdica és una representació esquemàtica de la disposició en una graella o taula, dels elements químics, amb un ordre determinat. |
 |
| La molècula d'aigua és un compost químic inorgànic format per dos àtoms d'hidrogen (H) i un àtom d'oxigen (O). Aquesta molècula és essencial per a la vida dels éssers vius. |
Actualment existeixen dispositius que ens permeten veure o mesurar elements a una resolució atòmica, és a dir, els àtoms. Les imatges que es presenten a continuació, en són exemples reals observats amb diferents microscopis d'escala atòmica.
 |
| Imatges a escala atòmica de diferents substàncies, obtingudes amb un Microscopi de Força Atòmica (AFM). |
Existeixen nivells microscòpics que permeten descomposar els àtoms en constituents encara més elementals, tot i que no es veuen amb cap microscopi. Aquests són:
- Electrons: partícules amb càrrega elèctrica negativa.
- Protons: partícules amb càrrega elèctrica positiva.
- Neutrons: partícules sense càrrega elèctrica.
A partir d'aquí, hi ha tot un conjunt de partícules subatòmiques que acaben finalment en els constituents últims de la matèria. Així, per exemple: els pions, els quarks o els gluons.
 |
| Primera imatge real d'un àtom d'hidrogen. |
 |
| Primera image en temps real, de dos àtoms vibrant dins d'una molècula |
Nivell macroscòpic
La matèria màssica es presenta en un dels quatre estats físics d'agregació molecular: sòlid, líquid, gasós i plasma.
D'acord amb la teoria cinètica molecular, la matèria es troba formada per partícules molt petites (molècules) que s'atreuen entre elles i es mouen contínuament.
La mobilitat de les partícules depèn de la temperatura, de manera que a mes temperatura, mes moviment tenen les partículas. Aquest grau de mobilitat és el factor que determina les propietats de la matèria i també justifica els canvis d'estat.
Per tant, l'estat físic d'una substància pot ser:
- Sòlid: les partícules esta situades de manera ordenada, unides per fortes forces d'atracció. Les partículas no es mouen, només vibren; per aquesta raó, els sòlids no canvien de forma ni de volum.
- Líquid: les partícules no estan unides les unes amb les altres amb tanta força i tenen la capacitat de fluir sense separar-se, de manera que canvien de forma, però no de volum.
- Gasós: les partícules s'atrauen molt dèbilment i poden separar-se molt les unes de les altres, de manera que tenen la capacitat de moure's lliurement a l'atzar i d'ocupar tot l'espai disponible.
- Plasma: es tracta d'un fluid similar a l'estat gasós, però que presenta presenta unes propietats diferents de les dels sòlids, líquids i gasos.
 |
| Lampada, bola o esfera de plasma. Inventada per Nikola Tesla, que la va anomenar: Inert Gas Discharge Tube (tub de descàrrega de gas inert). |
En física i química, s'anomena canvi d'estat a l'evolució de la matèria entre diversos estats d'agregació sense que hi hagi canvis en la seva composició.
Segons la teoria cineticomol.lecular explicada anteriorment, el paràmetre del qual depèn un cos per què es trobi en un estat o en un altre, és la temperatura, i també afavoreix la pressió:
- La temperatura: és una mesura de l'energia cinètica de les molècules i àtoms d'un cos. Un augment de la temperatura afavoreix la fusió, l'evaporació i la sublimació. Un descens de la tempeartura afavoreix els canvis oposats.
- La pressió: una reducció de la pressió afavoreix la fusió, l'evaporació i la sublimació, mentre que un descens afavoreix els canvis oposats.
3. Propietats de la matèria
La matèria té dos tipus de propietats:
- Propietats generals: són les propietats comunes a tota la matèria: la massa, el volum i la temperatura.
- Propietats específiques: són les propietats que permeten distingir una substància d'una altra. Per tant, aquestes depenen de la substància de què estan fets els cossos. Així, quan s'han de fer servir els materials per a diversos usos cal conèixer aquestes propietats per utilitzar el més idoni en cada cas. Són propietats específiques: la densitat, el color, l'olor i el sabor, etc.
Per altra banda, les propietats de la matèria que es poden mesurar s'anomenen magnituds. Són magnituds la massa, el volum, la longitud, o la velocitat.
Quan es mesura una magnitud se n'obté un valor que s'expresa amb dos elements: una quantitat representada amb un nombre i una unitat de mesura.
 |
| Taula on s'indiquen la unitats del SI, en què es mesuren les principals magnituds. |
Propietats generals
LA MASSA (m)
- És la quantitat de matèria que té un cos.
- És una magnitud fonamental.
- La unitat de massa en el SI és el quilogram (kg).
- Per mesurar la massa d'un cos sòlid, s'utilitzen les balances. De balances hi ha de molts tipus, segons la mida de l'objecte i la precisió amb què s'ha de fer la mesura. Les balances electròniques són molt precises i podem llegir directament la mesura en una pantalla.
- Per mesurar la massa d'un líquid o d'un gas, cal saber prèviament la massa del recipient que el conté; després es mesura la massa del recipient amb el líquid o el gas i es resten les dues mesures. La diferència que s'obté correspon a la massa del líquid o del gas.
EL VOLUM (V)
- És la quantitat d'espai que ocupa un cos.
- És una magnitud derivada de la longitud.
- La unitat de volum en el SI és el metre cúblic (m3).
- Per mesurar el volum d'un cos sòlid dependrà de la forma del cos: si és regular, s'apliquen les fórmules matemàtiques corresponents. Si és irregular, s'introdueix en un recipient graduat que contingui un volum conegut de líquid i es calcula la quantitat de líquid que desplaça el cos.
- Per mesurar el volum d'un líquid, utilitzem un recipient graduat: una proveta.
- Per mesurar el volum d'un gas cal tenir en compte que tindrà el mateix volum que el recipient que el conté, ja que els gasos tendeixen a ocupar sempre tot l'espai disponible.
 |
| Dues balances electròniques amb sal i sucre, i dues provetes amb aigua i alcohol. Sabries distingir totes les substàncies? Quines propietats generals estan mesurant? |
LA TEMPERATURA (Tª)
- Expressa la quantitat de calor que té un cos.
- És una magnitud fonamental.
- La unitat de temperatura en el SI és el kelvin (K), tot i que també s'utilitzen els graus Celsius (ºC). Per passar d'una escala a l'altra, hem de tenir en comte la relació que hi ha entre el punt de fusió i el punt d'ebullició:
- Per mesurar la temperatura d'un cos fem servir el termòmetre. De termòmetres hi ha de diversos tipus, però els més coneguts i utilitzats a la vida quotidiana es basen en el mateix principi: la dilatació d'una certa substància (alcohol acolorit), continguda en un tub estret graduat.
 |
| Els termòmetres digitals són aquells que utilitzen circuits electrónics per convertir en números les petites variacions de tensió obtingudes, mostrant finalment la temperatura en un visualitzador. |
Propietats específiques o característiques
LA DENSITAT (d)
- Expressa la quantitat de matèria (massa) que té un cos per unitat de volum.
- És una magnitud derivada.
- La densitat d'un cos es calcula fent el quocient entre la massa del cos, que s'expressa en quilograms, i el volum, que s'expressa en metres cúbics.
- Segons la densitat, els cossos són: pesants (quan hi ha molta quantitat de matèria per unitat de volum) o lleugers (quan hi ha poca quantitat de matèria per unitat de volum).
- Es pot comprovar que les substàncies sòlides són més denses que les líquides, i les líquides més que els gasos (a excepció del mercuri, que és un líquid més dens que la majoria dels sòlids).
 |
| Taula on s'indica la densitat d'algunes substàncies. |
 |
| La densitat de l'oli d'oliva és lleugerament inferior a la de l'aigua. És per això que quan les dues substàncies entren en contacte, es produeix un fenòmen com el de la imatge. |
EL PUNT DE FUSIÓ I D'EBULLICIÓ
Encara que una substància es trobi en un estat físic concret (líquid, sòlid o gasòs), aquest pot canviar amb la temperatura. L'estat físic d'una substància depèn del fet que la temperatura a la qual estigui sigui superior
- El punt de fusió: és la temperatura en què la substància passa de sòlida a líquida.
- El punt d'ebullició: és la temperatura en què la substància bull, és a dir, passa de líquida a gas.
EL COLOR, L'OLOR I EL SABOR
Algunes substàncies, tenen un color o olor o sabor tan característic que permet distingir-les de moltes altres a primer cop d'ull, olorada o tast. D'altres, en canvi, és més difícil distingir-les a partir únicament d'aquestes característiques...
Per tant, el color, l'olor i el sabor, no permeten distingir una substància d'altra, únicament per elles mateixes. A més, a vegades és difícil distingir-les perquè n'hi ha moltes del mateix color.
ALTRES PROPIETATS ESPECÍFIQUES:
DELS SÒLIDS:
- La duresa és la propietat de la matèria que indica la resistència que oposa un cos a ser ratllat o penetrat per altres cossos.
- La tenacitat és la propietat que tenen els materials de deformar-se considerablement abans de trencar-se.
- La fragilitat és la propietat contrària de la tenacitat. Un cos es fràgil quan es trenca abans de deformar-se.
- L'elasticitat és la propietat que permet a un material recuperar la forma inicial en deixar d'actuar-hi una forma que el deforma. Hi ha un límit a partir del qual el cos queda deformat permanentment. Aquest punt s'anomena límit d'elasticitat i és diferent per a cada material.
- La plasticitat és la propietat que té un material de deformar-se permanentment quan és pressionat.
- La ductilitat és la propietat que permet donar forma de fil prim a un material sense que aquest es trenqui.
- La mal·leabilitat és la propietat que té un material de deformar-se permanentment en forma de làmines o planxes primes quan és sotmès a un esforç.
- L'oxidabilitat és la capacitat d'alguns metalls d'alterar-se en contacte amb l'oxigen, generalment de l'aigua o de l'aire humit. Els materials que no s'oxiden s'anomenen inoxidables, com l'acer inoxidable.
- La conductivitat elèctrica indica la facilitat amb què el corrent elèctric circula a través d'un material. Quan un material no deixa passar l'electricitat es diu que és aïllant.
- La conductivitat tèrmica és la capacitat de deixar passar la calor. Quan un material no deixa passar la calor, també es diu que és aïllant.
DELS LÍQUIDS:
- La visositat és la capacitat que té un líquid de passar per un conducte prim. Si el líquid hi circula amb dificultat diem que es viscós, mentre que si flueix amb facilitat, diem que és fluid.
- La capil·laritat és la capacitat d'un líquid per amarar un sòlid porós o per ascendir per un tub estret. La capil·laritat depén del grau de viscositat del líquid i de les substàncies dissoltes que conté.
- La solubilitat és la capacitat d'una substància de dissoldre's en una altra, generalment un líquid. Per altra banda, els materials que no són solubles en un altre, s'anomenen insolubles.
- Què vol dir dissoldre's? Ja sabem que una substància està formada per partícules. Si pensem en un líquid, entre les partícules que el formen hi ha espais que poden ser ocupats per partícules d'una altra substància. Quan això passa diem que aquesta substància es dissol en el líquid. Per tant, com més quantitat de líquid tinguem, més espais podran ser ocupats per una altra substància.
DELS GASOS:
- La difusió consisteix en la dispersió i el repartiment uniforme dels gasos en una altra substància, ja sigui un sòlid, un líquid o un gas.
- La dilatació consisteix en l'augment de volum del gas, quan aquest s'escalfa. Si el gas perd temperatura llavors es contrau. Els líquids també presenten aquesta propietat, en major grau que els sòlids, però en menor grau que els gasos.